Carbonsäureester: physikalische Eigenschaften und Bedeutung
Download Carbonsäureester (PDF, 272 KB)
Download Carbonsäureester (DOC, 52 KB)
Download Carbonsäureester (ODT, 85 KB)
Download Carbonsäureester Lösung (PDF, 439 KB)
Download Carbonsäureester Lösung (DOC, 67 KB)
Download Carbonsäureester Lösung (ODT, 90 KB)
Tab. 1: Bedeutung
| Ausgangsstoffe | Ester(typ) | Vorkommen | Verwendung |
|---|---|---|---|
| Niedere Alkansäuren + niedere Alkohole |
Aromastoffe | Früchte, Wein | Nahrungsmittelzusätze, Lösungsmittel für Lacke |
| Alkansäuren + Glycerin | Fette (Triglyceride) | Pflanzen- und Tiergewebe | Nahrungsmittel, Seifen |
| Höhere Alkansäuren und höhere einwertige Alkohole | Wachse | Pflanzen, Tiere (Biene, Schaf) | Kerzen, Bodenpflege, Lanolin als Cremezusatz |
| Polyalkansäuren + Polyalkohole | Polyester | (synth. Herstellung) | Textilfasern (Diolen, Trevira), Gießharze, Kunststoffe |
| Essigsäure + Cellulose | Celluloseacetat | - | Acetatseide, Filme, Folien, Lacke |
| Salpetersäure + Cellulose | Glycerintrinitrat (= Nitroglycerin) | - | Sprengstoff, Herzmedikament |
| Salpetersäure + Cellulose | Cellulosenitrat (Schießbaumwolle) | - | Nitrolacke, Celluloid |
ÜA 1: Benennen Sie die folgenden Beispiele für Aromastoffe:
Methansäure + Ethanol ⇄ Methansäureethylester Rumaroma + H2O
Butansäure + Pentanol ⇄ Butansäurepentylester Aprikosenaroma + H2O
Butansäure + Ethanol ⇄ Butansäurethylester Ananasaroma + H2O
Pentansäure + Pentanol ⇄ Pentansäurepentylester Apfelaroma + H2O
ÜA 2: Begründen Sie die Siedetemperaturen der Verbindungen im folgenden Diagramm (alle Molekülmassen ca. 100 u) !!!
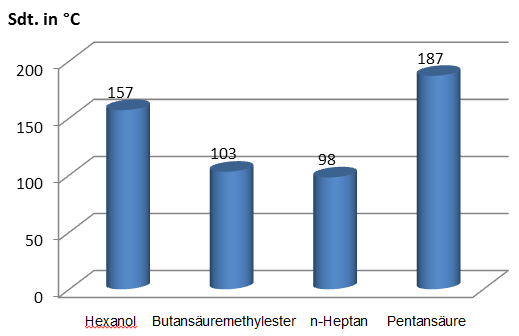 |
n- Heptan: kleinste Sdt., da nur VDWK. Sdt. Ester > Sdt. Heptan, da zusätzlich Dipol-Dipol-WW ausgebildet werden können. Sdt. Hexanol > Sdt. Ester, da zusätzlich H-Brücken vorhanden. Höchste Sdt. Pentansäure, bildet H-Brücken (+ Dimere, dadurch höhere VDWK) |
ÜA 2:Beurteilen Sie Löslichkeit und Schmelztemperatur der Verbindungen a. – d. anhand ihrer Molekülstruktur!
a. niedere Ester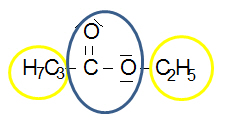 = Aromastoffe |
Löslichkeit:schlecht wasserlöslich, da unpolar Smt./Sdt.:niedrig, da keine H-Brücken ausgebildet werden, leicht flüchtig (→ Geruchs-, Aromastoffe) |
b. höhere Ester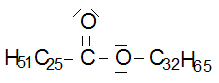 = Wachse, z. B. Bienenwachs |
Löslichkeit:unpolar, lange Alkylreste überwiegen Smt./Sdt.:durch lange Alkylreste höhere VDWK, fest |
c. Monoglyceride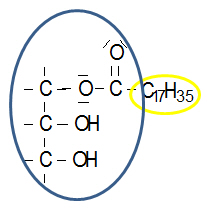 = Emulgator |
Löslichkeit:hydrophiler Molekülbereich („Kopf“, OH-Gruppen) und lipophiler Molekülbereich („Schwanz“, Alkylgruppen), stabilisiert Emulsionen (z. B. in Fertigsoßen, Backwaren, Cremes und Lotionen) |
d. Triglyceride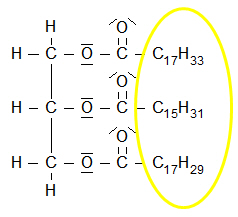 = Fette |
Löslichkeit:unpolarer Bereich überwiegt, mehrere lange Alkylketten Smt./Sdt.:Schmelzbereich steigt mit zunehmender Länge der Fettsäurereste (im Detail siehe Thema Fette) |


