Milch – Versuche – Milchsorten
Versuch 1: Entrahmung
Grundlagen
Rohmilch bildet beim Stehen schon nach 30 – 60 Minuten eine sichtbare Rahmschicht. Ursache ist der Dichteunterschied zwischen der Milchflüssigkeit und den Fettkügelchen. Es tritt hierbei keine Zerstörung der Emulsion ein, es ändert sich nur das Verteilungsgleichgewicht der Fettkügelchen. Eine weitere Möglichkeit des Aufrahmens ist das Zentrifugieren, das wesentlich schneller geht.
Beim Zentrifugieren wird eine Emulsion oder eine Suspension in ein starkwandiges Reagenzglas gegeben und in eine Zentrifuge gehängt. Durch eine schnelle Rotation entsteht eine Fliehkraft, wobei der Stoff mit der größeren Dichte ganz außen an den Boden des Reagenzglases „flieht“.
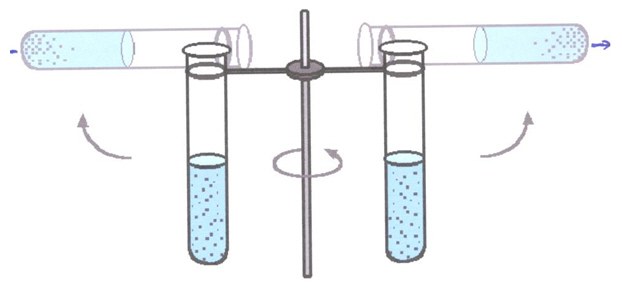
Die Trennung von Sediment und Überstand erfolgt nach dem Zentrifugieren durch Dekantieren.
Materialien
- Zentrifuge und Zentrifugengläser
- Milch, Sahne, Rohmilch
Durchführung
- Zentrifugengläser bis zu 3/4 mit der Probe füllen
- gleichmäßig in die Zentrifuge einordnen
- bei 6.500 Umdrehungen 6 Minuten zentrifugieren
Beobachtung
Ergebnis
Versuch 2: Milch als Emulsion
Grundlagen
Emulsionen sind disperse Systeme zweier oder mehrerer ineinander unlöslicher Flüssigkeiten. Eine der flüssigen Phasen bildet dabei das Dispersionsmittel, in dem die anderen Phasen in Form feiner Tröpfchen verteilt sind.
Es kommen die beiden Emulsionstypen Öl in Wasser (O/W) und Wasser in Öl (W/O) vor. Beispiele aus dem Alltag für O/W-Emulsionen sind Milch, Mayonnaise oder Körperlotion, für W/O-Emulsionen Butter, Margarine oder Salben. Der Durchmesser der dispergierten Tröpfchen in Emulsionen liegt zwischen 10-2 und 10-6 cm, die meisten Emulsionen zeigen eine uneinheitliche Teilchengröße und sind damit polydispers.
In der Milch sind die Lipide (Fettanteile) mit Proteinen und Phospholipiden umgeben, die als Emulgator wirken.
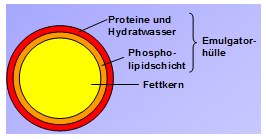
Nur O/W-Emulsionen sind mit Wasser ohne Phasentrennung verdünnbar, was gleichzeitig als einfacher Nachweis für diesen Emulsionstyp dient.
2.1 Anfärben von Butter
Mit dem Versuch soll gezeigt werden, dass Butter eine W/O-Emulsion ist.
Material
- Projektionsmikroskop
- Objektträger
- Deckgläser
- Mörser
- Butter
- Sudanrot B (lipophil)
- Methylenblau (hydrophil)
Durchführung
Im Mörser wird ein Stück Butter mit einer Spatelspitze Sudanrot B und einer Spatelspitze Methylenblau gut verrieben. Die so angefärbte Butter wird unter dem Mikroskop betrachtet. Es sind deutlich die rötlich angefärbte Fettphase und die darin blau angefärbten Wassertropfen erkennbar.
2.2 Tyndall-Effekt
Grundlagen
Milch ist eine Emulsion von Fetttröpfchen im Milchplasma (wässrige Milchlösung ohne Fett).
Da der Durchmesser der Fetttröpfchen im Bereich der Wellenlängen des sichtbaren Lichts liegt, streuen sie einfallendes Licht (Tyndall-Effekt). Ein Lichtstrahl, der durch eine Lösung von wenigen Tropfen Milch in Wasser fällt, ist als Kegel zu erkennen.
Materialien
- Becherglas, hohe Form (250 ml)
- Pasteurpipette
- Taschenlampe/Laserpointer
- schwarzes Tonpapier
- Schere
- Klebstreifen
- Milch
- Wasser
Durchführung
Das Becherglas wird bis unter den Rand mit Wasser gefüllt und mit wenigen Tropfen Milch versetzt. Das schwarze Papier wird trichterförmig gerollt, so dass eine Öffnung von 1 cm Durchmesser entsteht und mit einem Klebestreifen befestigt. Der Raum wird verdunkelt (Licht aus!). Das Licht der Taschenlampe wird durch die Trichteröffnung auf das Becherglas geleitet. Der Strahlengang wird als Kegel sichtbar.
Versuch 3: Hitzebehandlungen
Grundlagen
Durch die Hitzebehandlung der Milch werden pathogene Krankheitskeime abgetötet, Proteine denaturiert und Enzyme inaktiviert. Diese Inaktivierung der Enzyme ist eine Möglichkeit den Grad der Erhitzung festzustellen.
3.1 Xanthinoxidase in Milch
Materialien
- 2 Reagenzgläser groß
- Wasserbad 40 °C
- Messpipetten 5 ml
- Rohmilch
- pasteurisierte Milch
- Formaldehyd-Lösung (0,4 %)
- Methylenblau-Lösung (0,04 % in Wasser)
- Paraffinöl
Durchführung
In zwei Demonstrationsreagenzgläser werden je 20 ml Milch gegeben (1x Rohmilch, 1x pasteurisierte Milch). Anschließend gibt man in beide Gläser je 3 ml Formaldehyd-Lösung und 2 ml Methylenblau-Lösung, dann überschichtet man zum Sauerstoffausschluss etwa 2 cm hoch mit Paraffinöl. Beide Reagenzgläser werden in ein Wasserbad (40 °C) gestellt.
Auswertung
Nach etwa 5 Minuten beobachtet man eine Entfärbung des Reaktionsgemisches, das Rohmilch enthält, während das Gemisch mit pasteurisierter Milch blau bleibt.
Rohmilch enthält das sog. Schardinger-Enzym, eine Aldehyd-Dehydrogenase. Das Enzym überträgt Wasserstoff von Formaldehyd auf Methylenblau, welches zum farblosen Leukomethylenblau reduziert wird. Da das Schardiger-Enzym bei Erhitzen auf 60 °C zerstört wird, fehlt es in der pasteurisierten Milch, es tritt dort keine Entfärbung ein. Diese Reaktion wird auch in der Molkereitechnik zum Nachweis der Pasteurisierung angewendet.
3.2 Peroxidasenachweis in Milch nach Storch
Grundlagen
Lactoperoxidase katalysiert den Abbau von Wasserstoffperoxid. Der dabei freigesetzte atomare Sauerstoff oxidiert eine farblose 1,4-Phenylendiamin-Lösung zu violettem Indoamin (Storchsche Reaktion). Die Intensität der Färbung ist proportional zur Enzymkonzentration.
Positive Peroxidasereaktion: 30 Sekunden nach dem Durchmischen färbt sich pasteurisierte Milch blau.
Negative Peroxidasereaktion: 30 Sekunden nach dem Durchmischen kein Farbumschlag.
Materialien
Probenröhrchen mit Verschluss (mind. 15 ml)
- 5 ml, 10 ml Vollpipette
- 5 ml Messpipette
- 2 x 100 ml Messkolben
- dunkelbraune Flasche
- 1,4-Phenylendiamin
- Schwefelsäure konz.
- 30%iges Wasserstoffperoxid
Herstellung der Lösungen
a) 1,4-Phenylendiamin-Lösung
2 g 1,4-Phenylendiamin ( C6H8N2 ) werden im warmen Wasser (50 °C) gelöst und auf 100 ml aufgefüllt. Die Lösung wird in einer dunkelbraunen Flasche mit Glasstopfen kühl und dunkel aufbewahrt. 1,4-Phenylendiamin-Lösung bildet innerhalb von 1 – 2 Tagen nach dem Ansetzen einen Niederschlag, der zu entfernen ist.
b) Wasserstoffperoxid-Lösung
9 ml Wasserstoffperoxid mit einem Massenanteil von ca. 30 % werden in Wasser gelöst und auf 100 ml aufgefüllt. Zur Stabilisierung wird 1 ml konzentrierte Schwefelsäure je Liter Lösung zugegeben. Wasserstoffperoxid-Lösung ist einen Monat haltbar, sofern sie in einer Flasche mit Glasstopfen als Schutz gegen organische Verbindungen im Dunkeln aufbewahrt wird.
Durchführung
- 5 ml der Milchprobe in ein sauberes Probenröhrchen mit geeignetem Verschluss geben
- 5 ml 1,4-Phenylendiamin-Lösung dazu geben
- zwei Tropfen Wasserstoffperoxid-Lösung zugeben
Auf den 30 Sekunden nach dem Durchmischen auftretenden Farbumschlag ist zu achten. Ein später als 30 Sekunden nach dem Zusatz der Reagenzien auftretender Farbumschlag ist eine unspezifische Reaktion.
3.3 Peroxidasenachweis mit Guajaktinktur
Durchführung
Versetzen Sie die unterschiedlich hitzebehandelten Proben mit Guajaktinktur.
Ergebnis
In der Rohmilch zeigt eine Blaufärbung Peroxidase an. H-Milch zeigt keine Blaufärbung, da die aktive Peroxidase bei Temperaturen von über 80 °C zerstört wird.
3.4 Nachweis der alkalischen Phosphatase
a) mit Lactognost-Reagenz
b) mit Testreagenz
Versuch 4: Homogenisierung
Grundlagen
Milch wird homogenisiert, um die Absetzgeschwindigkeit der Fetttröpfchen zu verringern. Die Milch wird dafür durch feine Düsen gepresst, wodurch die Größe der Fett-Tröpfchen deutlich verringert und die Emulsion stabilisiert wird. Die Homogenisierung kann in der Schule mit Hilfe eines Pflanzensprengers veranschaulicht werden.
Materialien
- Pflanzensprenger
- 2 Schraubdeckelgläser
- Messzylinder
- Salatöl
- Wasser
Durchführung
In zwei Schraubdeckelgläsern werden jeweils 8 ml Salatöl mit 200 ml Wasser versetzt. Nach dem Verschließen werden beide Gefäße gleich stark geschüttelt. Der Inhalt des einen Gefäßes wird dann rasch in den Pflanzensprenger überführt und durch die Sprengerdüsen zurück in das Schraubglas gesprüht. Beide Emulsionen werden nun optisch untersucht; die Absetzgeschwindigkeit der Fetttröpfchen in beiden Emulsionen wird verglichen.
Beobachtung
Ergebnis
Versuch 5: Verkostungen verschieden erhitzter Milchsorten
Die Schülerinnen und Schüler erhalten eine Reihe nummerierter Gläser/Becher, die mit unterschiedlichen Milchproben gefüllt wurden sowie eine Liste der verwendeten Milchsorten.
Z. B.
- frische Vollmilch, pasteurisiert, homogenisiert, 3,5 % Fett
- H-Milch, homogenisiert, 1,5 % Fett
- Milch mit natürlichem Fettgehalt, pasteurisiert, homogenisiert
- Sterilmilch
- Vollmilch, pasteurisiert, homogenisiert, länger haltbar, 3,5 % Fett
Durch Betrachtung des Erscheinungsbildes und Verkostung der Milchsorten wird eine Zuordnung vorgenommen.
Auswertung
|
Milchprobe |
1 |
2 |
3 |
4 |
5 |
|
Milchsorte A - E |
|
|
|
|
|


